中学受験の理科~気体の発生や金属の燃焼で確認する化学計算問題の基本
ユーチューブによるワンポイント・レッスンを行っております。重要ポイントを1テーマ2分で解説するものです。次々と公開していきますので、チャンネル登録をお願いします。
⇒ ユーチューブによるワンポイント・レッスン
△上のリンクをクリック△
2022/12/08

化学の計算問題といえば、中心となるのは「中和」「溶解度」なのですが、どのテーマにおいても考え方の基本は比例計算です。
「中和」と「溶解度」については2冊目の図書「【伝家の宝刀】力学・天体・化学計算の解法」で徹底的に解説しましたが、ここでは比例計算に慣れるため、「気体の発生」と「金属の燃焼」を取りあげてみます。
本格的な化学計算問題に移るための準備運動として、気軽に取りくんでみてくださいね。こんな感じの計算問題もあるんだ、と知っておくだけで充分でしょう。
本番までに与えられた時間の量は同じなのに、なぜ生徒によって結果が違うのか。それは、時間の使いかたが異なるからです。どうせなら近道で確実に効率よく合格に向かって進んでいきましょう! くわしくは、以下からどうぞ。
⇒ 中学受験 理科 偏差値アップの勉強法
気体の発生に関する計算問題
計算問題を始める前に、気体の発生(酸素および二酸化炭素)における基本を確認しておきましょう。以下の記事を、ご覧ください。
⇒ 中学受験の理科 気体の発生
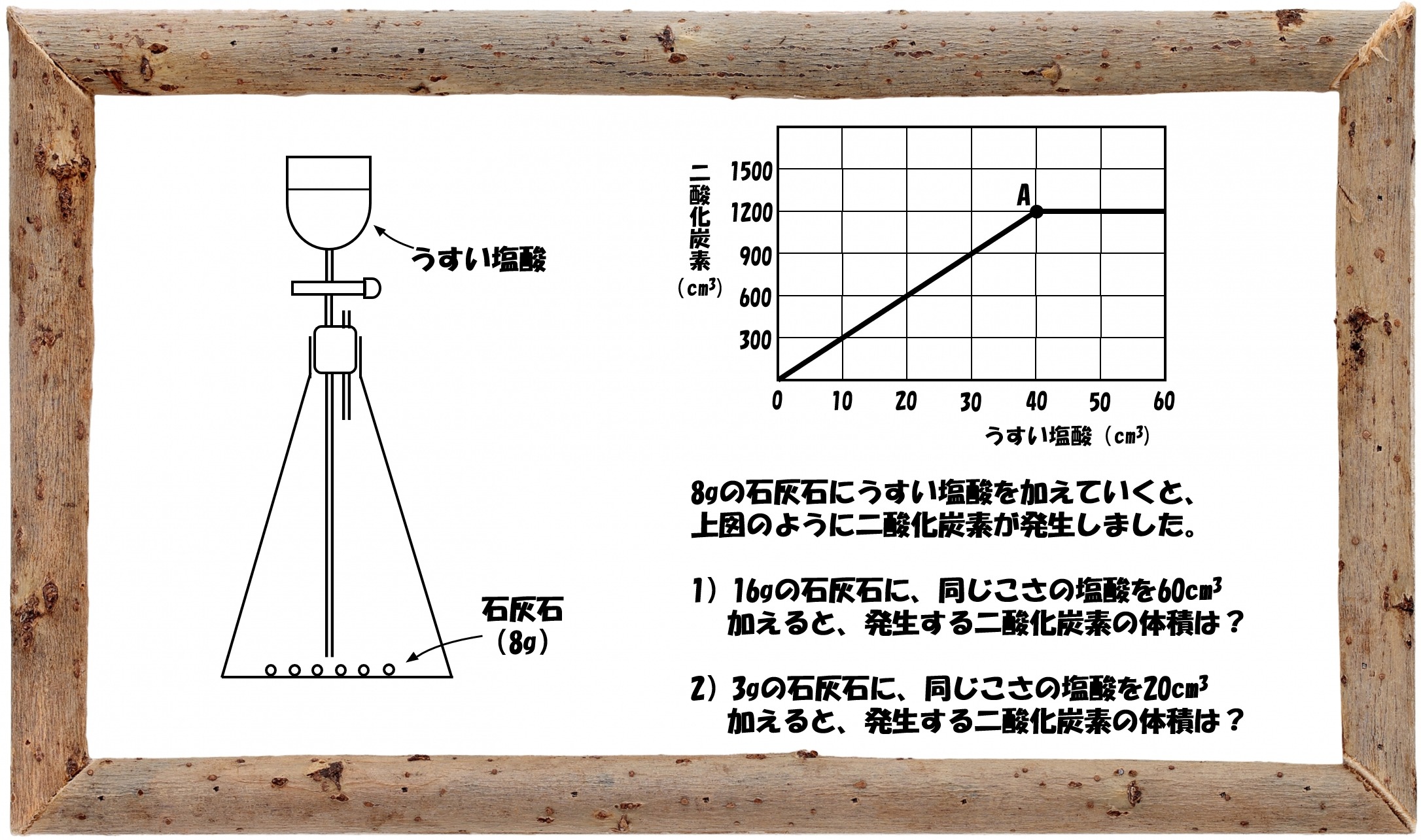
この計算問題では、ある一定量の石灰石が待ちかまえていて、うすい塩酸を加えていきます。うすい塩酸の量が多いほど、発生する二酸化炭素も多くなりますが、やがて石灰石がなくなって気体の発生は止まるわけです。
グラフから、石灰石が残っているかぎり「うすい塩酸を加える量」と「発生する二酸化炭素」の関係は正比例であり、A点で石灰石がなくなったのだと分かります。
化学計算問題で最も重要なことは、最初につかまえる量です。「登場する物質」と「量」との関係をつかまえるわけですが、この計算問題で登場するのは「石灰石」「うすい塩酸」「二酸化炭素」の3つだけ。これら3者の量的な関係が分かるのはA点のみとなります。
たとえばグラフから、「うすい塩酸20cm3を加えて、二酸化炭素600cm3が発生する」ことは明らかですが、そのときに反応した石灰石の量は分かりません。
つまり、A点より前の部分では石灰石が残っているため、何gの石灰石が反応したのか分からないし、A点より後では塩酸が残っている状態なのです。

したがって、A点における、「石灰石8gと、うすい塩酸40cm3がちょうど反応して、二酸化炭素1200cm3が発生した。」をつかまえることになります。
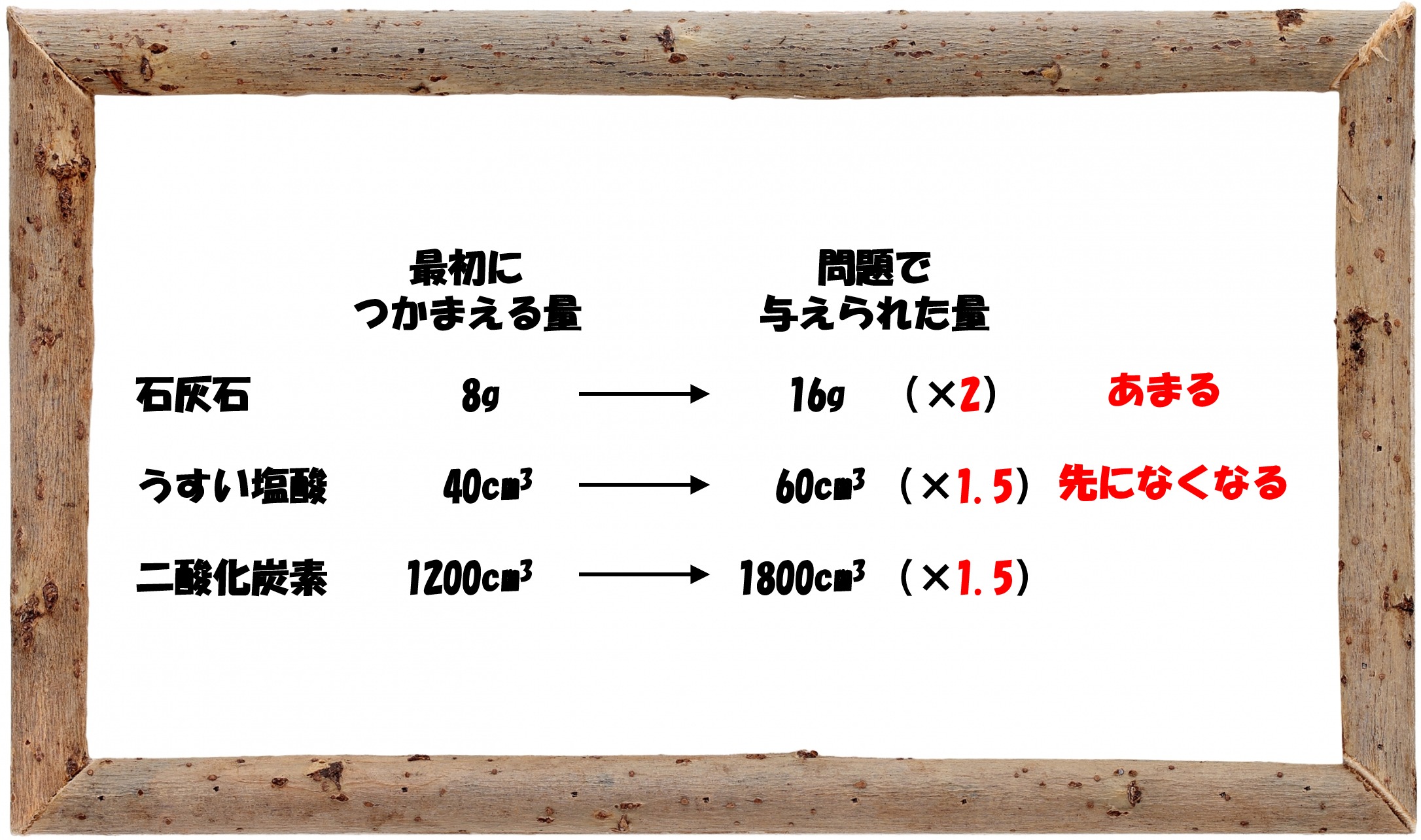
つかまえてしまえば、あとは問題で与えられる量から比例計算で答えを求めるだけ。最初の問題では、「石灰石16g」と「うすい塩酸60cm3」が与えられています。
.jpg)
石灰石はつかまえた量の2倍、うすい塩酸は1.5倍ですから、さきになくなるのは塩酸(少ないほう)のはずですね。つまり二酸化炭素は、つかまえた量の1.5倍(1200×1.5=1800cm3)発生して、反応が止まることになります。
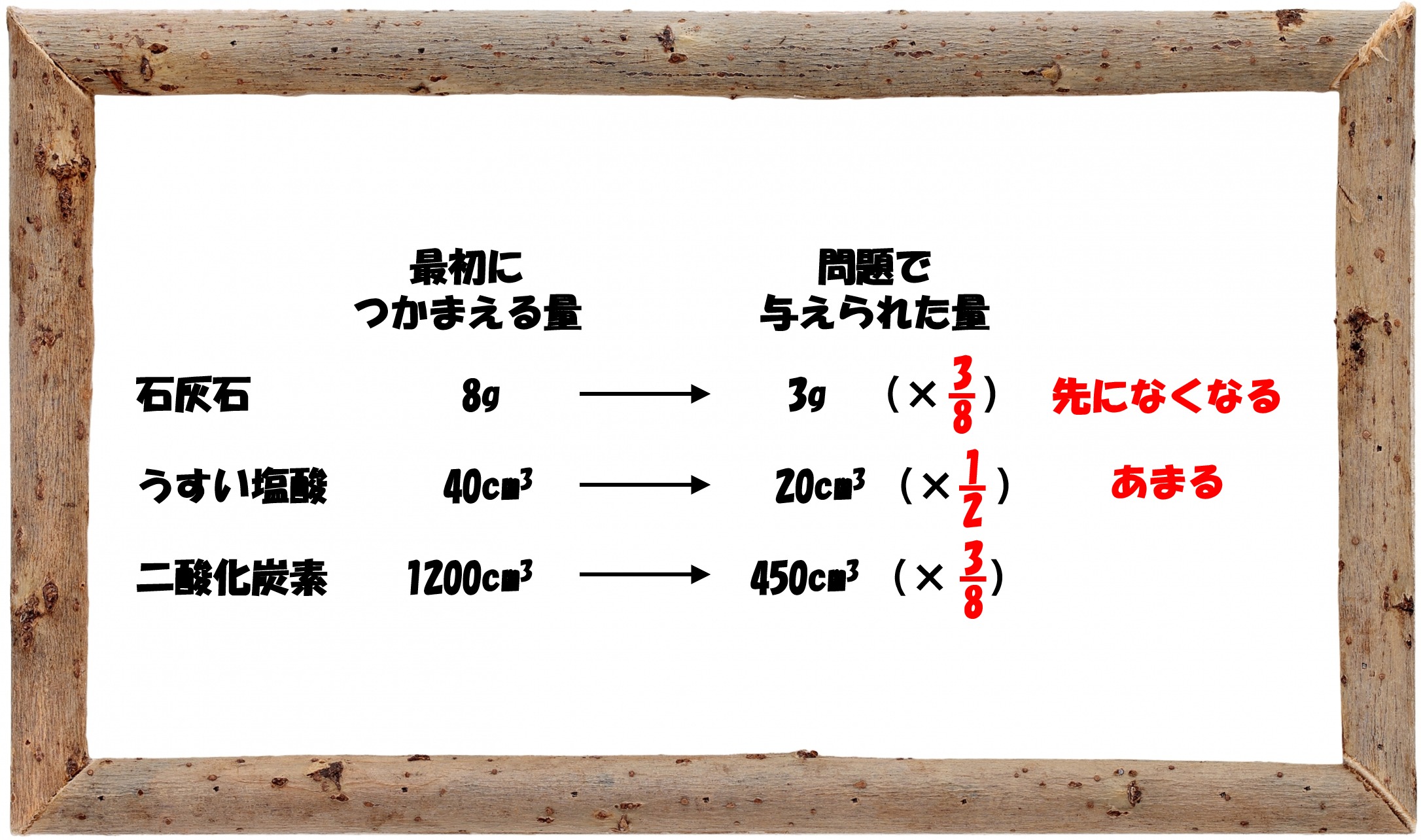
次の問題では、「石灰石3g」と「うすい塩酸20cm3」が与えられています。石灰石はつかまえた量の「8分の3倍」、うすい塩酸は「2分の1倍」ですから、さきになくなるのは少ない石灰石。したがって二酸化炭素は、つかまえた量の「8分の3倍」である450cm3(1200×8分の3)発生して、反応が止まります。
金属の燃焼に関する計算問題
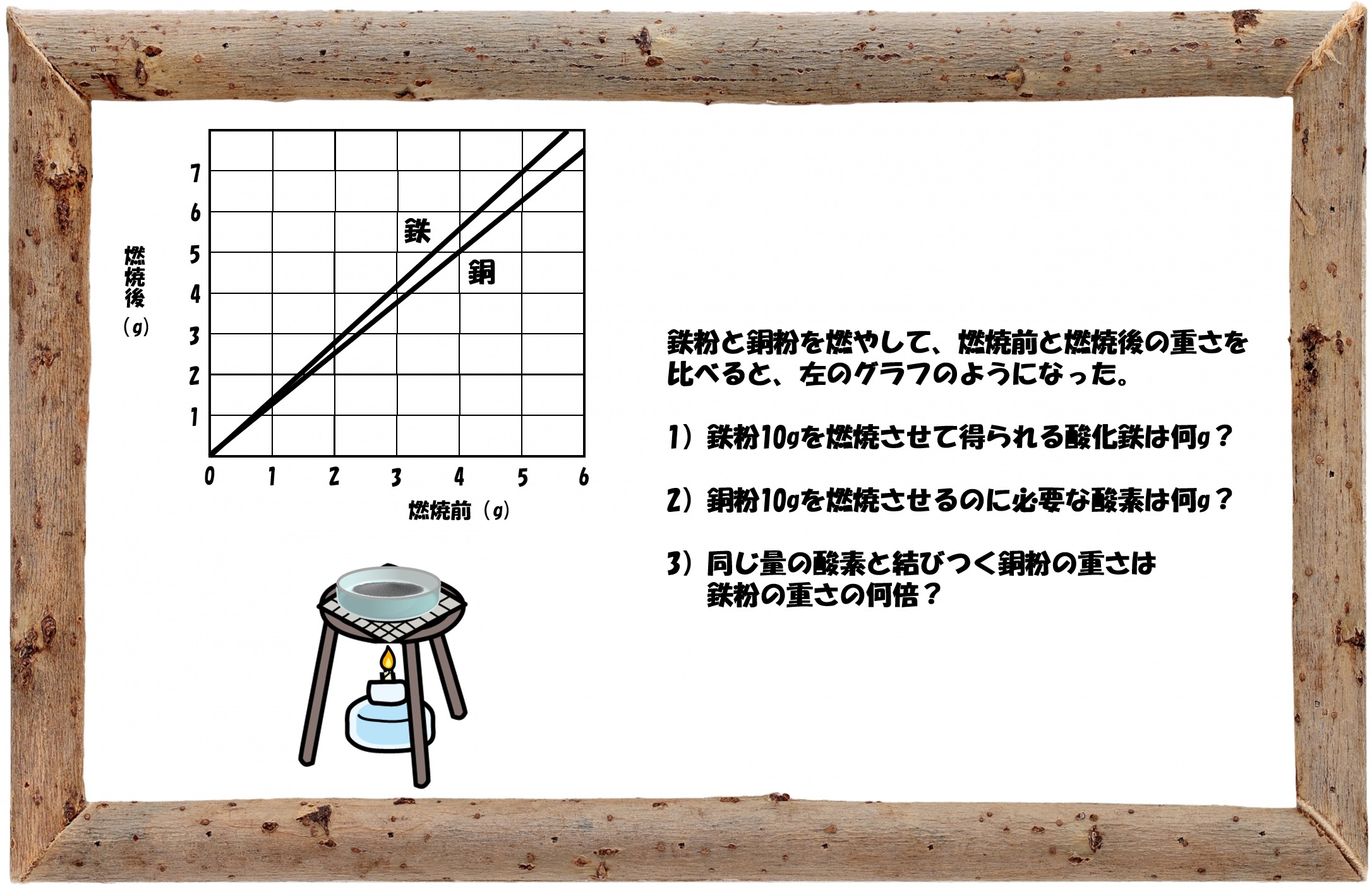
金属が燃焼するというのは、イメージしにくいかもしれませんが、物は発火点より高い温度で酸素があれば燃えるので、金属も燃焼します。燃焼とは酸素と結びつくことですから、燃焼後は結びついた酸素の分だけ重くなるわけです。
グラフから、5gの鉄が燃焼すると、燃焼後(酸化鉄)は7gとなることが分かります。登場するのは、「鉄粉(燃焼前)」「鉄粉(燃焼後)」「酸素」の3つ。つまり、鉄粉5gに対して、2gの酸素が結びついたことになりますね。最初の問題では、これをつかまえておくわけです。
問題で与えられた量は、鉄粉10gですから、つかまえた量の2倍。つまり、「鉄粉(燃焼後)」も「結びついた酸素」も2倍になります。
「気体の発生」と違って、ここでは登場する「酸素」がなくなることを考える必要がありませんから、楽ですね。
なお、この問題では、「鉄粉(燃焼後)=酸化鉄」の量(答えは14g)が問われていることに注意してください。

次の問題は、銅粉です。グラフから、4gの銅が燃焼すると燃焼後は5gとなるので、1gの酸素と結びつくことが分かります。そして、与えられた量は、銅粉10gです。
この問題では、酸素の量(答えは2.5g)を問われていることに注意してください。

最後の問題は、同じ量の酸素と結びつく金属(燃焼前)の重さの比です。何が条件で、何を問われているのか、それさえ間違えなければ正解できますね。
鉄粉と銅粉で酸素の量を合わせると、「鉄粉(燃焼前):銅粉(燃焼前)」=「1:1.6」であることが分かります。
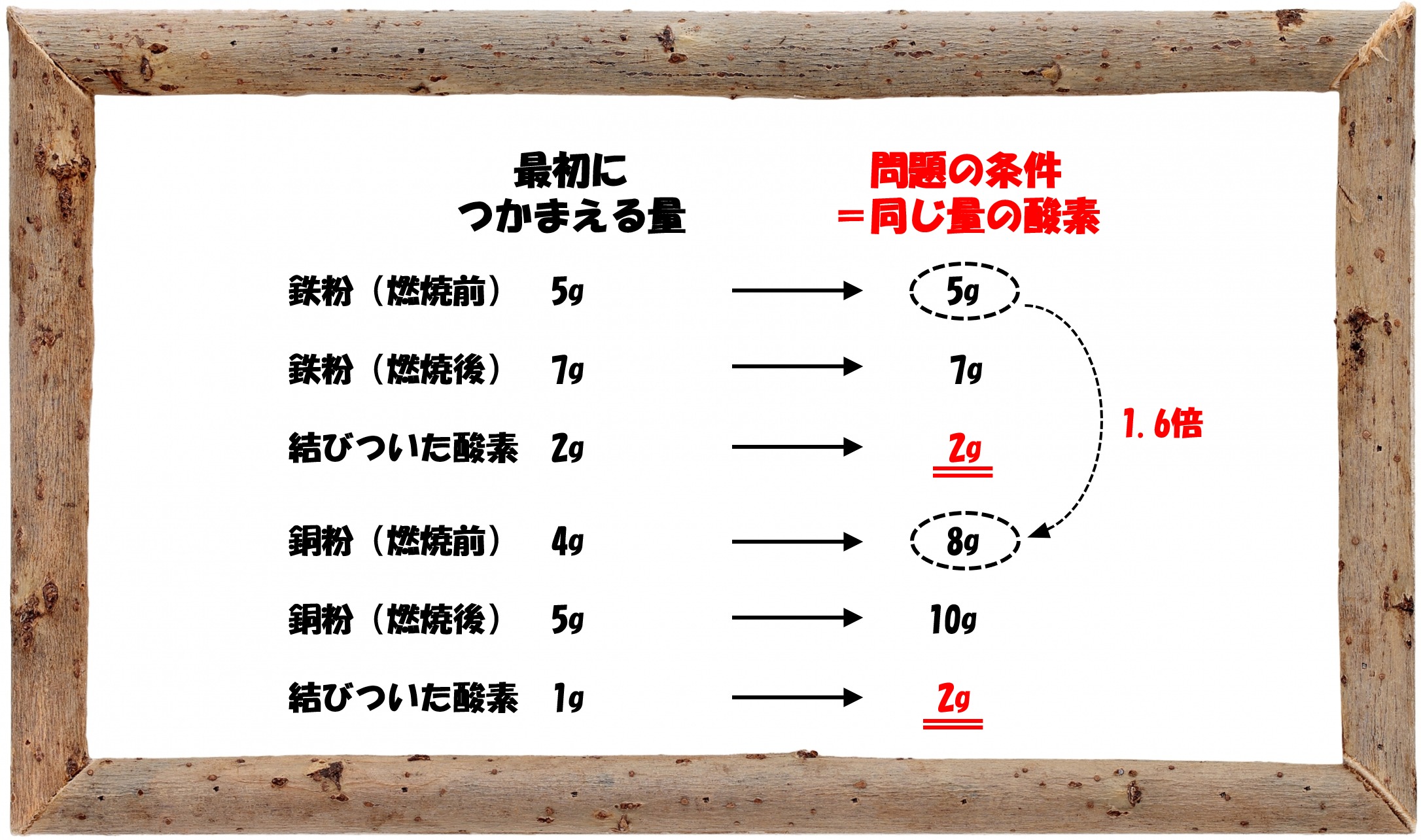
以上のように化学計算問題では、最初につかまえるべき量とは何なのか、それこそが最重要ポイントであることを忘れないでくださいね。
次はいよいよ、化学の基本固めである「ろうそくの燃焼」です。以下の記事を、ご覧ください。
⇒ 中学受験の理科 ろうそくの燃焼~この理解で受験対策は完ペキ!
2020年10月の赤本・2021年11月の青本に続き、2022年12月エール出版社から、全国の書店で偏差値アップの決定版ついに公開!
くわしくは、以下の記事をご覧ください。
⇒ 中学受験 理科 偏差値アップの勉強法
スポンサーリンク
スポンサーリンク
